Cambios fÃsicos y cambios quÃmicos
Las modificaciones en la presión, la temperatura o las interrelaciones de las sustancias, pueden originar cambios fÃsicos o quÃmicos en la materia.
Cambios fÃsicos de la materia:
Son aquellos cambios que no generan la creación de nuevas sustancias, lo que significa que no existen cambios en la composición de la materia, como se ve en la figura siguiente.
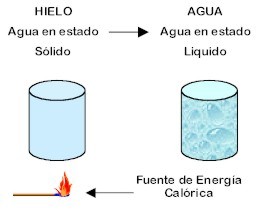
El cambio fÃsico se caracteriza por la no existencia de reacciones quÃmicas y de cambios en la composición de la materia.
Cambios quÃmicos:
Son aquellos cambios en la materia que originan la formación de nuevas sustancias, lo que indica que existieron reacciones quÃmicas.
El cambio QuÃmico de la materia se caracteriza por la existencia de reacciones quÃmicas, de cambios en la composición de la materia y la formación de nuevas sustancias.
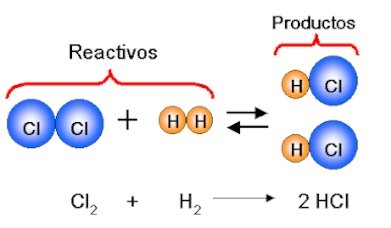
Cambio QuÃmico de la materia: Formación de Ãcido ClorhÃdrico, mediante la reacción de Cloro e Hidrógeno.
Observe que en los cambios quÃmicos la materia sometida al cambio posee unas caracterÃsticas diferentes a la materia inicial.
Composición y propiedades de la materia
Como se vio anteriormente, la materia presenta tres estados fÃsicos, dependiendo de factores ambientales como la presión y la temperatura; independiente de ello, el aspecto de la materia está determinado por las propiedades fÃsico-quÃmicas de sus componentes, encontrándose materia homogénea y materia heterogénea.
Materia homogénea
Es aquella que es uniforme en su composición y en sus propiedades y presenta una sola fase, ejemplo de ello serÃa un refresco gaseoso, la solución salina, el Cloruro de Sodio o sal de cocina; este tipo de materia se presenta en formas homogéneas, soluciones y sustancias puras.
Materia heterogénea
Es aquella que carece de uniformidad en su composición y en sus propiedades y presenta dos o más fases, ejemplo de ello serÃa la arena, el agua con aceite; este tipo de materia es también conocida como mezcla y se caracteriza por el mantenimiento de las propiedades de los componentes y la posibilidad que existe de separarlos por medio de métodos fÃsicos.
Sustancias puras, elementos y compuestos
Sustancia pura
Una sustancia es pura cuando se encuentra compuesta por uno o más elementos en proporciones definidas y constantes y cualquier parte de ella posee caracterÃsticas similares, definidas y constantes; podrÃamos decir que una sustancia es pura cuando se encuentra compuesta en su totalidad por ella y no contiene cantidades de otras sustancias; ejemplos de ello serÃan la sacarosa, el agua, el oro.
Elemento:
Sustancia pura imposible de descomponer mediante métodos quÃmicos ordinarios, en dos o más sustancias, ejemplo: el Hidrógeno (H), el OxÃgeno (O), el Hierro (Fe), el Cobre (Cu).
Compuesto:
Sustancia pura posible de descomponer mediante métodos quÃmicos ordinarios, en dos o más sustancias, ejemplos: El agua (H2O), la sal (NaCl), el ácido Sulfúrico (H2SO4).
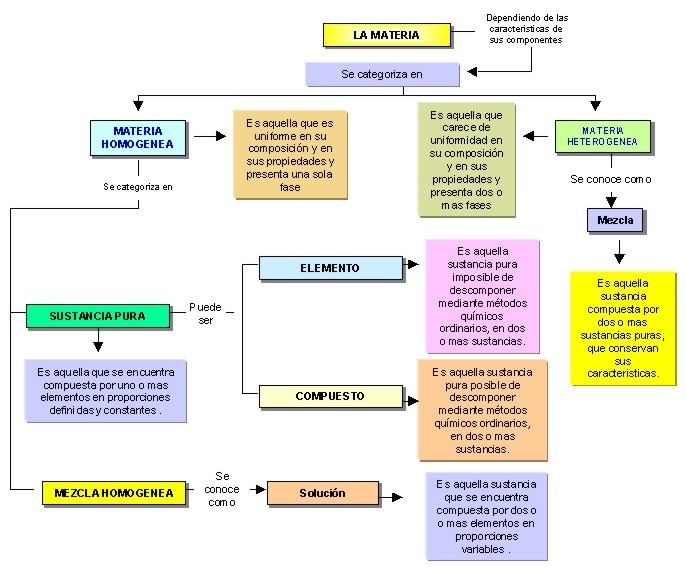
Mapa conceptual que muestra la categorización de la materia, dependiendo de las caracterÃsticas y composición de las sustancias constituyentes.